- 2014年05月23日
- 大鵬薬品工業株式会社
新規抗悪性腫瘍剤「ロンサーフ®配合錠」薬価収載ならびに新発売のお知らせ
大鵬薬品工業株式会社(本社:東京、代表取締役社長:小林 将之)は、抗悪性腫瘍剤「ロンサーフ®配合錠T15・T20」(一般名:トリフルリジン・チピラシル塩酸塩、開発コード:TAS-102、以下本剤)が、本日薬価収載されましたことをお知らせします。発売は5月26日(月)を予定しています。
本剤は、大鵬薬品が創製した経口のヌクレオシド系抗悪性腫瘍剤であり、国内第Ⅱ相臨床試験結果に基づき、「治癒切除不能な進行・再発の結腸・直腸癌(標準的な治療が困難な場合に限る)」を効能・効果として、本年3月24日に世界に先駆けて国内で製造販売承認を取得しました。
また、治癒切除不能な進行・再発の結腸・直腸がん患者を対象に実施されている国際共同第Ⅲ相臨床試験(試験名:RECOURSE)において、本剤がプラセボ投与群に対し、主要評価項目である全生存期間を有意に延長する結果が得られました。この結果に基づき、今後欧米においても申請を予定しています。
大鵬薬品は、標準的な治療が困難で治癒切除不能な進行・再発の結腸・直腸がんに対し、 本剤が新たな選択肢の一つとして、患者さんの治療に貢献できることを期待しています。
【ロンサーフについて】
本剤は、トリフルリジン(FTD)とチピラシル塩酸塩(TPI)を配合した経口のヌクレオシド系抗悪性腫瘍剤です。FTDはDNAの複製時にチミジンの代わりに直接DNA鎖に取り込まれ、DNAの機能障害を引き起こして抗腫瘍効果を発揮すると推測されています。TPI はFTDの分解に関与するチミジンホスホリラーゼを阻害し、FTDの血中濃度を維持します。
【RECOURSEについて】
本試験は、無作為割付・二重盲検・プラセボ対照の国際共同臨床第Ⅲ相試験で、日本の他、北米、欧州、オーストラリアから800名の患者登録がありました。対象は少なくとも2種類以上の標準化学療法(フッ化ピリミジン系薬剤、イリノテカン、オキサリプラチン、ベバシズマブ、KRAS遺伝子に変異のない野生型の場合では抗EGFRモノクローナル抗体)に不応となった治癒切除不能な進行・再発の結腸・直腸がん患者です。本剤の有効性を検証することを目的に、患者さんを本剤投与群又はプラセボ投与群にランダムに割り付けました。主要評価項目は全生存期間です。
製品概要
| 製 品 名 | ロンサーフ®配合錠T15、ロンサーフ®配合錠T20 |
|---|---|
| 一 般 名 | トリフルリジン・チピラシル塩酸塩 |
| 効能・効果 | 治癒切除不能な進行・再発の結腸・直腸癌(標準的な治療が困難な場合に限る) |
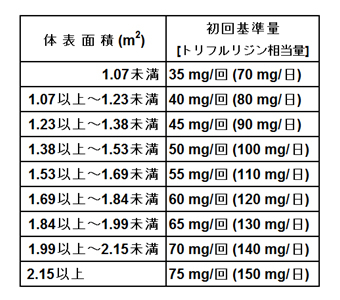
| 用法・用量 | 通常、成人には初回投与量(1回量)を体表面積に合わせて次の基準量とし(トリフルリジンとして約35mg/m2/回)、朝食後及び夕食後の1日2回、5日間連続経口投与したのち2日間休薬する。これを2回繰り返したのち14日間休薬するこれを1コースとして投与を繰り返す。なお、患者の状態により適宜減量する。 |
| 製造承認日 | 2014年3月24日 |
|---|---|
| 薬価収載日 | 2014年5月23日 |
| 発売予定日 | 2014年5月26日 |
| 包 装 | ロンサーフ®配合錠T15:PTP包装:20錠(10錠× 2)、60錠(10錠× 2 × 3) ロンサーフ®配合錠T20:PTP包装:20錠(10錠× 2)、60錠(10錠× 2 × 3) |
| 薬 価 | ロンサーフ®配合錠T15:2,489.60円 ロンサーフ®配合錠T20:3,340.90円 |
| 製造販売元 | 大鵬薬品工業株式会社 |
ニュースリリースに記載されている内容は、報道発表日現在の情報です。
当社のニュースリリースは、報道関係者への情報提供を目的としています。医療用医薬品や開発品に関する情報を含む場合がありますが、これらはプロモーション、広告、医療上のアドバイスを目的としたものではありません。
